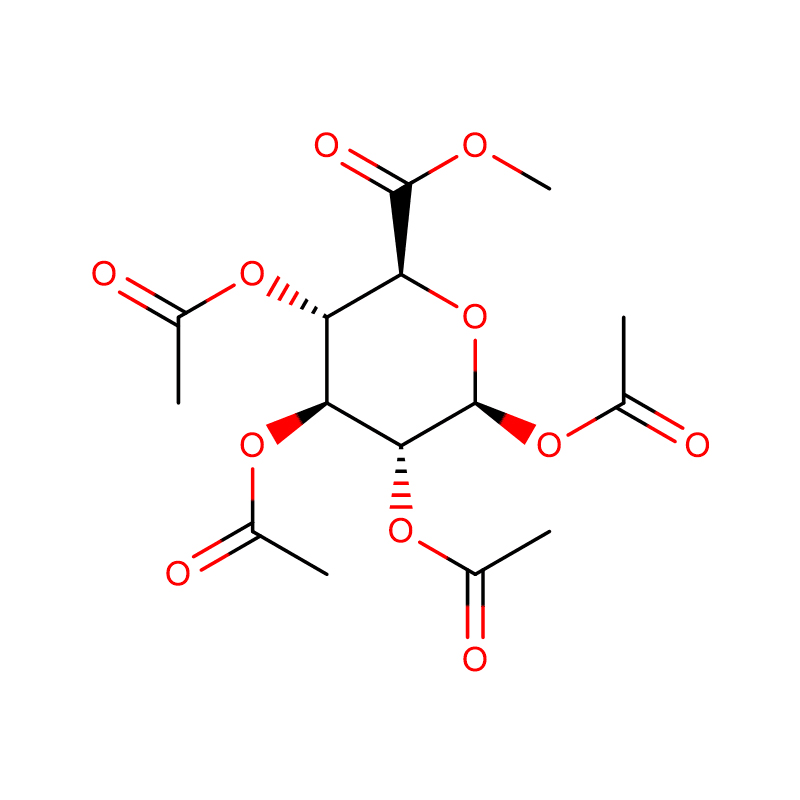
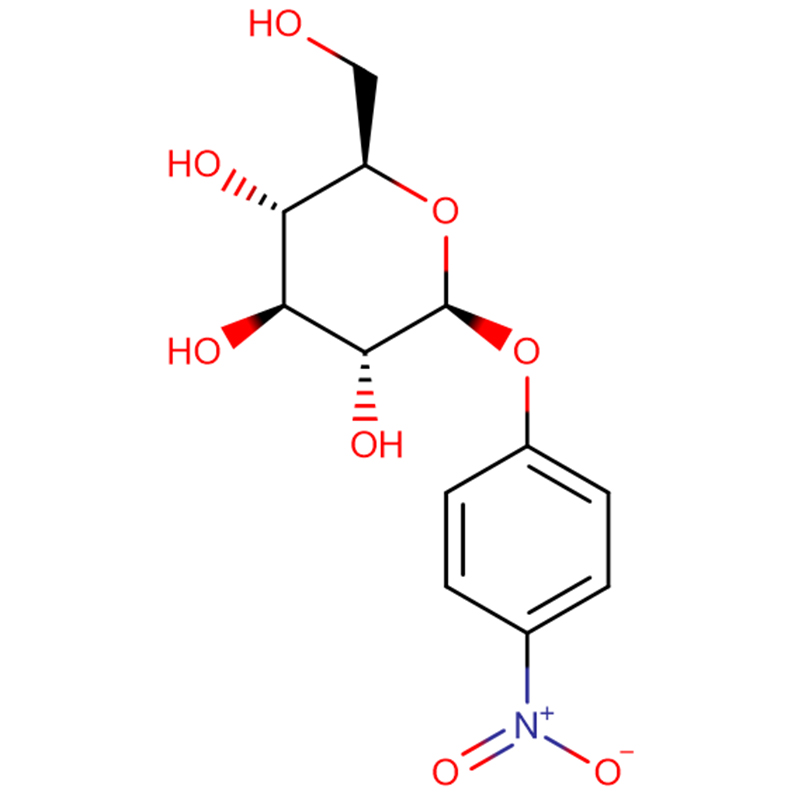
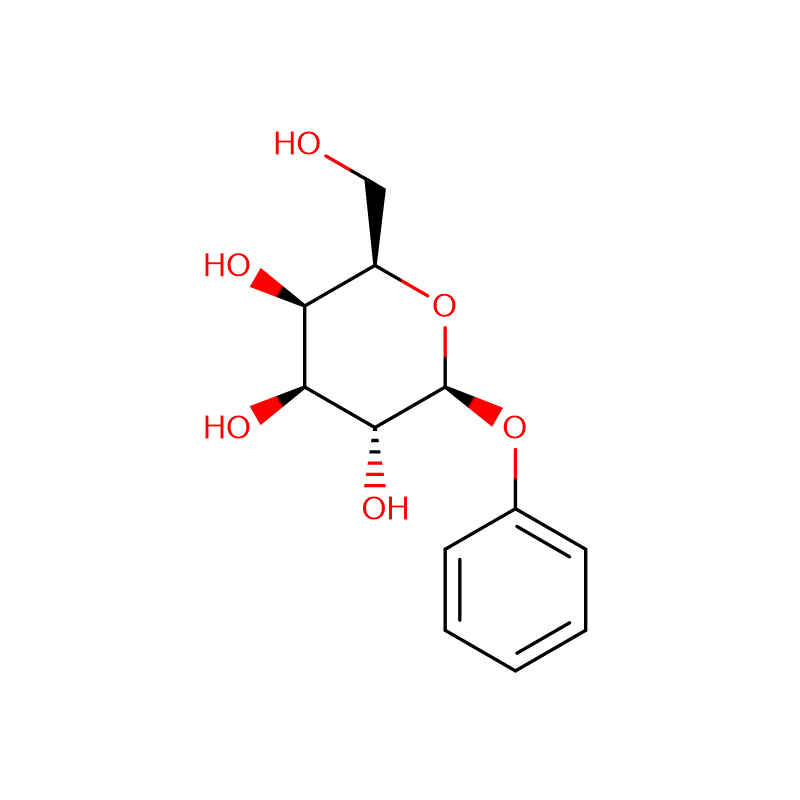
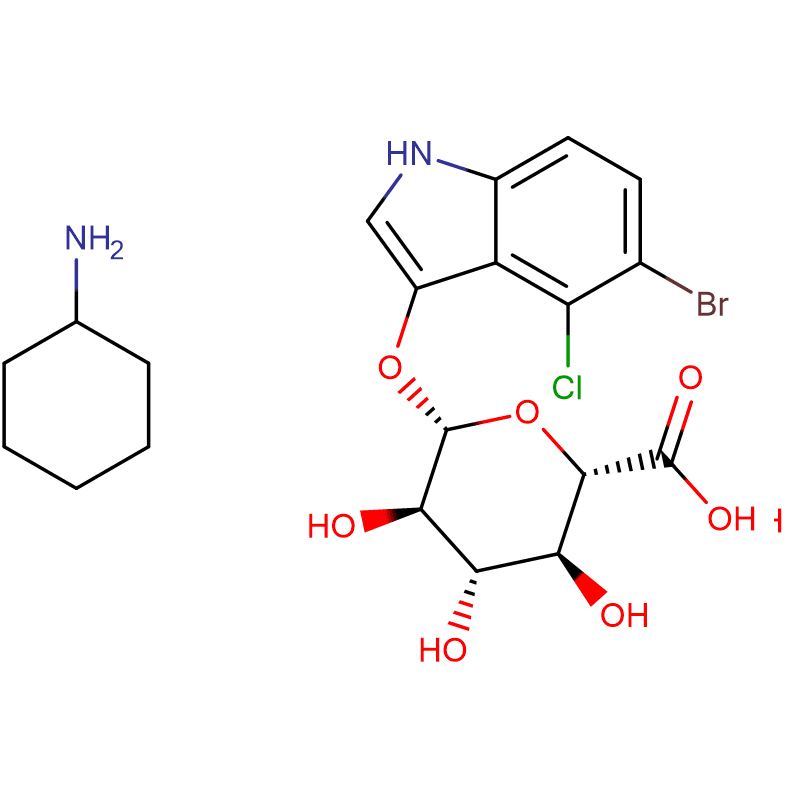
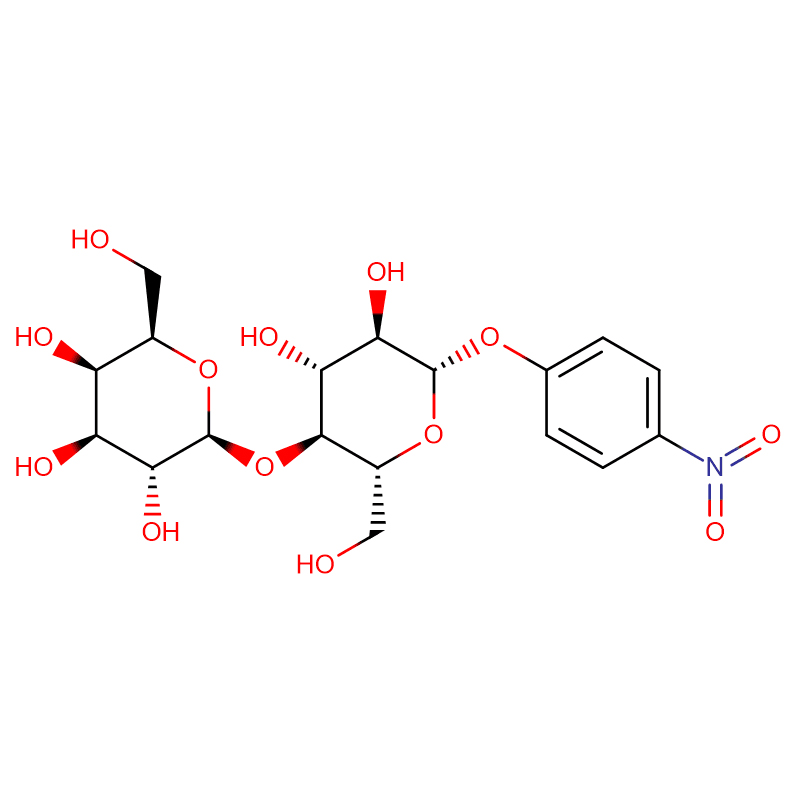
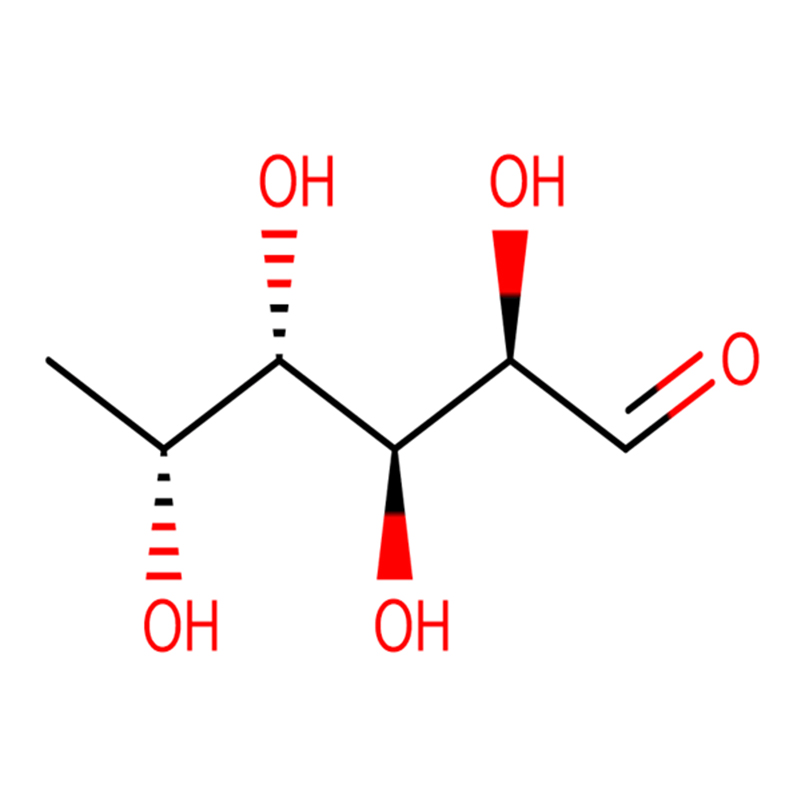
Два изомерни бицикло[4.1.0]хептанови аналози на инхибитора на гликозидазата галакто-валидамин, (1R*,2S,3S,4S,5S,6S*)-5-амино-1-(хидроксиметил)бицикло[4.1.0]хептан -2,3,4-триол, са синтезирани в 13 стъпки от 2,3,4,6-тетра-О-бензил-D-галактоза.Инхибиторните активности на двата конформационно ограничени амина и съответните им ацетамиди бяха измерени срещу търговски алфа-галактозидазни ензими от кафеени зърна и Е. coli.Активността на ензима GH27 от фамилията гликозил хидролаза (кафеено зърно) е конкурентно инхибирана от 1R,6S-амин (7), свързващо взаимодействие, което се характеризира със стойност на K(i) от 0,541 микроМ.Алфа-галактозидазата GH36 E. coli показва много по-слабо свързващо взаимодействие с 1R,6S-амина (IC(50)= 80 микроМ).Диастереомерният 1S,6R-амин (9) се свързва слабо с двете галактозидази, (кафеено зърно, IC(50)= 286 микроМ) и (Е. coli, IC(50)= 2,46 тМ).