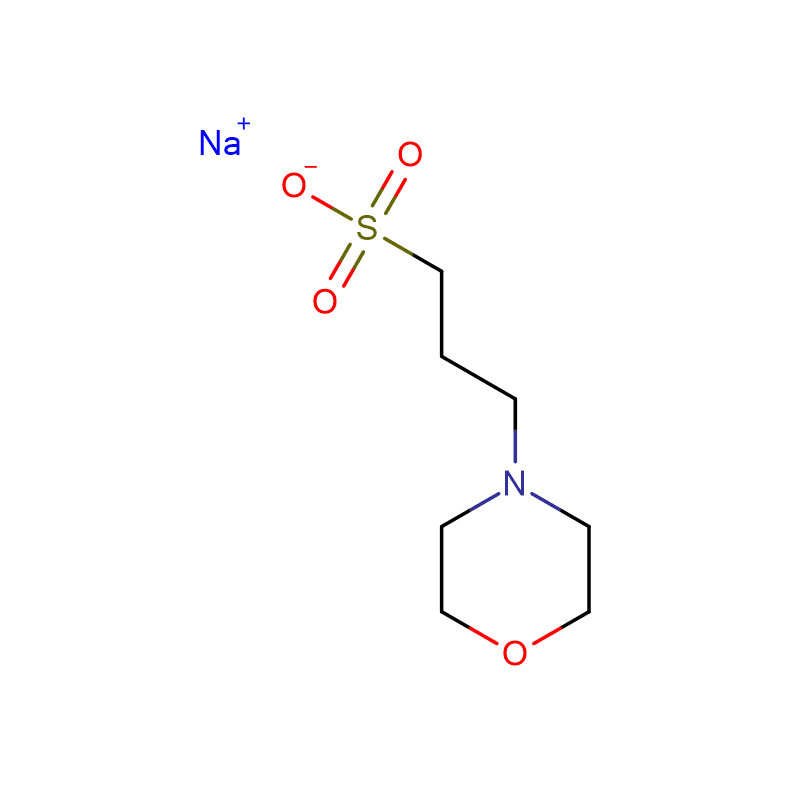
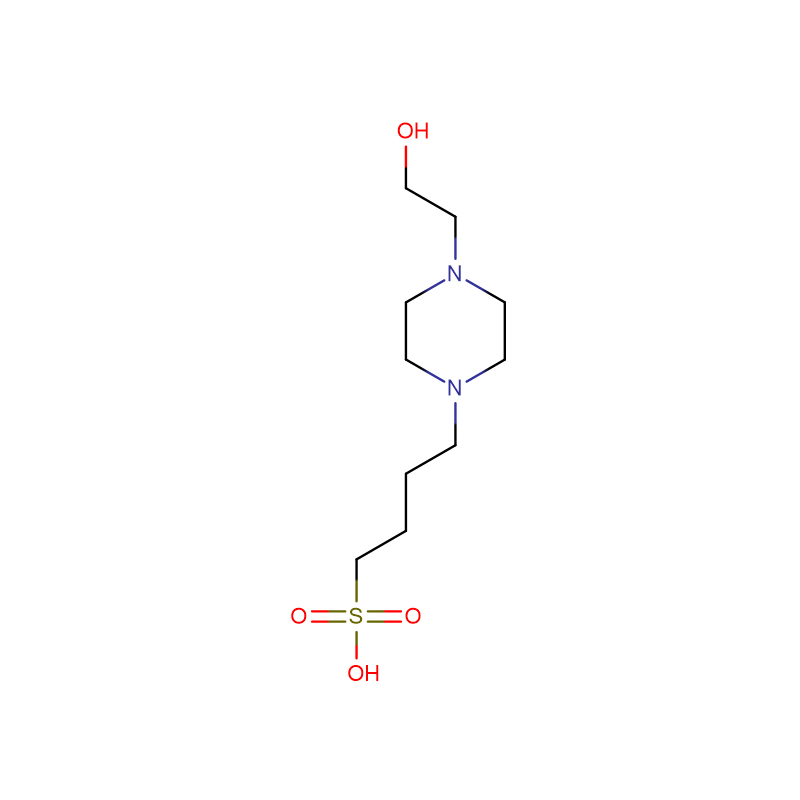
HEPBS Cas:161308-36-7 N-(2-хидроксиетил)пиперазин-N'-(4-бутансулфонова киселина) Бял кристален прах 99%
| Каталожен номер | XD90100 |
| Име на продукта | HEPBS |
| CAS | 161308-36-7 |
| Молекулярна формула | C10H22N2O4S |
| Молекулно тегло | 266,36 |
| Подробности за съхранение | Околна среда |
| Хармонизиран тарифен код | 2933599090 |
Спецификация на продукта
| Външен вид | Бял кристален прах |
| Ассаy | ≥ 99% |
| Температура на съхранение | Съхранявайте на RT |
| Точка на топене | 211-216°С |
| Коефициент на киселинност (pKa) | 8,3 (при 25 ℃) |
Ние разбираме значението на защитата на целостта на вашите биомолекули и реагенти с правилните буферни системи.Нашите биологични буфери осигуряват стабилност на разтвора и контрол на pH, без да се намесват в биологичните процеси, и доставят критични соли и хранителни вещества за клетките и тъканите.Нашите усъвършенствани буферни системи могат да ви осигурят феноменална стабилност в клетъчни култури, полимеразна верижна реакция (PCR), скрининг на лекарства, биообработка, пречистване и приложения на крайни формули.Всички наши продукти могат да бъдат мащабирани от ранни изследвания до търговски приложения в различни буферни степени.Предлагаме множество конфигурации на опаковки, смесване по поръчка и дори течна формула.
Ние също така доставяме изчерпателна селекция от висококачествени биохимикали в практична гама от степени и в разнообразие от иновативни, удобни за потребителя опции за опаковане.В допълнение към готовите продукти, ние предлагаме производство на реагенти по поръчка, смесване и опаковане, за да отговорим на вашите нужди.
Принципът на работа и стойността на рН на буферния разтвор Когато към някои разтвори се добави определено количество киселина и основа, това има ефект на възпрепятстване на промяната на рН на разтвора, което се нарича буферен ефект.Такъв разтвор се нарича буферен разтвор.Смесени разтвори на слаби киселини и техните соли (като HAc и NaAc) и смесени разтвори на слаби основи и техните соли (като NH3·H2O и NH4Cl) са буферни разтвори.Буфериращият ефект на буферния разтвор, съставен от слабата киселина НА и нейната сол NaA върху киселината, се дължи на наличието на достатъчно количество алкали А- в разтвора.Когато определено количество силна киселина се добави към този разтвор, Н-йоните основно се консумират от А-йони: така че рН на разтвора остава почти непроменено;когато се добави определено количество силна основа, слабата киселина НА, присъстваща в разтвора, консумира OH- йони, които възпрепятстват промяната на pH.



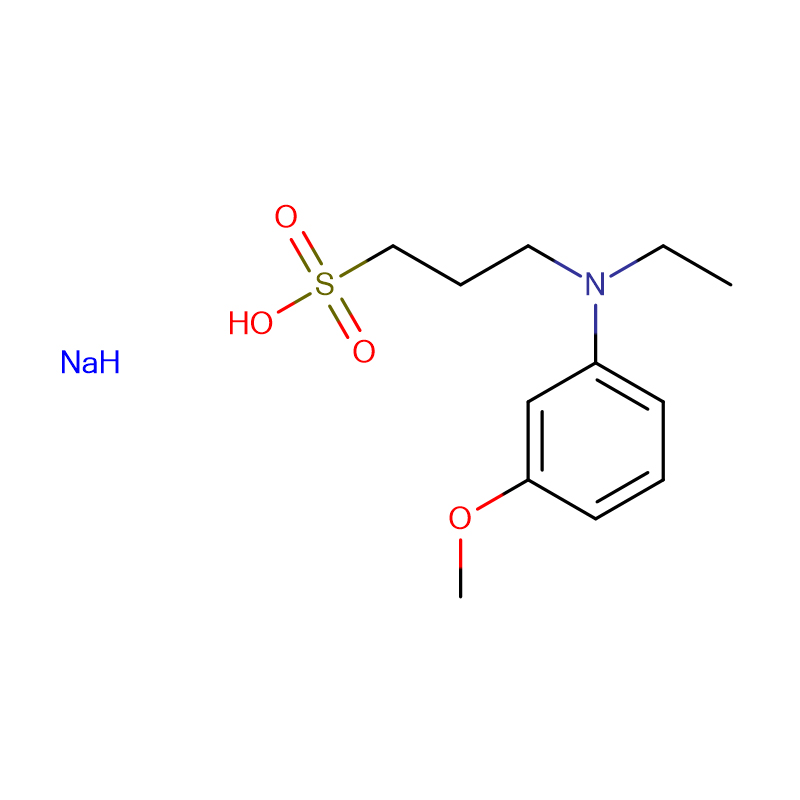
![TAPS-NA Cas:91000-53-2 Течна 99% N-[Трис(хидроксиметил)метил]-3-аминопропансулфонова киселина натриева сол](http://cdn.globalso.com/xdbiochems/91000-53-2.jpg)